
胆膵がんに対する早期診断・新規治療の研究開発
ご支援のお願い
東京大学医学部附属病院 消化器内科の胆膵グループでは、胆膵がん(胆道がん・膵がん)の診療に日々取り組んでいますが、診断・治療ともに十分な成績が得られているとは言えません。難治がんである胆膵がんの治療成績の向上を目指して、我々は短期・長期的な視野と多角的なアプローチからunmet needsの克服を目指しています。具体的には膵がん早期診断のための新規バイオマーカーを探索する研究、膵がんの高危険群である膵嚢胞に対するより効率的なサーベイランス法を確立するための研究、さらには腹膜播種を伴う膵がんや切除不能進行胆道がんに対する新たな抗がん剤治療の臨床研究および基礎研究を実施しています。
これらの研究は公的な競争的資金や東京大学医学部附属病院の研究費を用いて実施していますが、皆様のご支援を得ることができれば、より質の高い研究を迅速に実施することが可能になります。最難治がんである胆膵がんの治療成績を向上するためにも、早期診断・新規治療の開発に向けた研究に対する、皆様のご支援を賜りますようお願い申し上げます。
東京大学医学部附属病院
消化器内科 特任講師 高原 楠昊
プロジェクト概要
胆膵がんは発病初期には自覚症状に乏しいため、“沈黙の臓器“のがんとして恐れられています。根治的な手術が望めない進行した状態で診断されることが多く、また手術できたとしても高率に再発することから、満足のいく治療成績は得られていません。これらのがんは近年増加傾向にあり、早期診断ならびに新規治療開発は喫緊の課題のひとつとなっています。私たちは多角的なアプローチにより胆膵がんにおけるunmet needsの克服を目指しています。
腹膜播種を伴う膵がんに対する腹腔内治療について
腹膜播種(腹膜への転移)は膵がんに好発する転移形態で、最も重要な予後規定因子のひとつです。しかし、腹膜播種の制御に注目した治療開発は不十分で、近年の化学療法の進歩にも関わらず、経時的な予後延長が得られていません。そのため、私たちは標準的な治療に新しい抗がん剤治療である腹腔内化学療法を併用する治療法を開発し、これまで東京大学基金に設置した「スキルス胃癌、膵癌、大腸癌に対する腹腔内化学療法の研究開発」基金を通じた多くのご支援により、現在、全国の6施設の協力を得て「腹膜播種を伴う膵癌に対するゲムシタビン/ナブ-パクリタキセル点滴静注+パクリタキセル腹腔内投与併用療法」の臨床研究を先進医療の制度下に遂行中です。腹膜播種の制御と治療成績向上のためには、治療効果を予測する革新的なバイオマーカーの確立に加えて、腹腔内化学療法に対する耐性獲得のメカニズム解明とその克服が必要不可欠であると考えています。そのために患者さんから得られる臨床検体を用いて探索的な検討も進めています。このような、腹腔内化学療法の研究開発に加えて、次のステップとして、胆膵がんに対する早期診断・新規治療の実現に向けた多角的アプローチによる研究開発を行うために、胆膵がんに絞った基金を設置してこの度、支援をお願いする次第です。
膵がんの早期診断を目指したバイオマーカーの探索
膵がんは特異的な症状に乏しいため、臨床症状を早期発見の指標とすることは困難です。そのため健診等による定期的な画像検査が提案されていますが、一般人口における膵がんの有病率は低いため、膵がんの高危険群を対象としたスクリーニングが必要と考えられています。近年の画像診断装置の機能向上に伴い、膵のう胞が指摘される機会が増加しています。膵のう胞は膵がんの危険因子のひとつであり、各種ガイドラインで定期的な画像検査の必要性が強調されていますが、その悪性化の頻度は年率0.5-1%程度と比較的低く、繰り返しの画像検査を行い続けることも負担となるため、より簡便で低コストなサーベイランス法の確立が求められています。
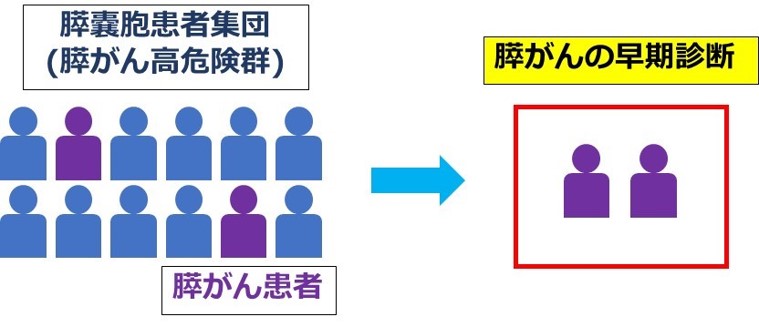
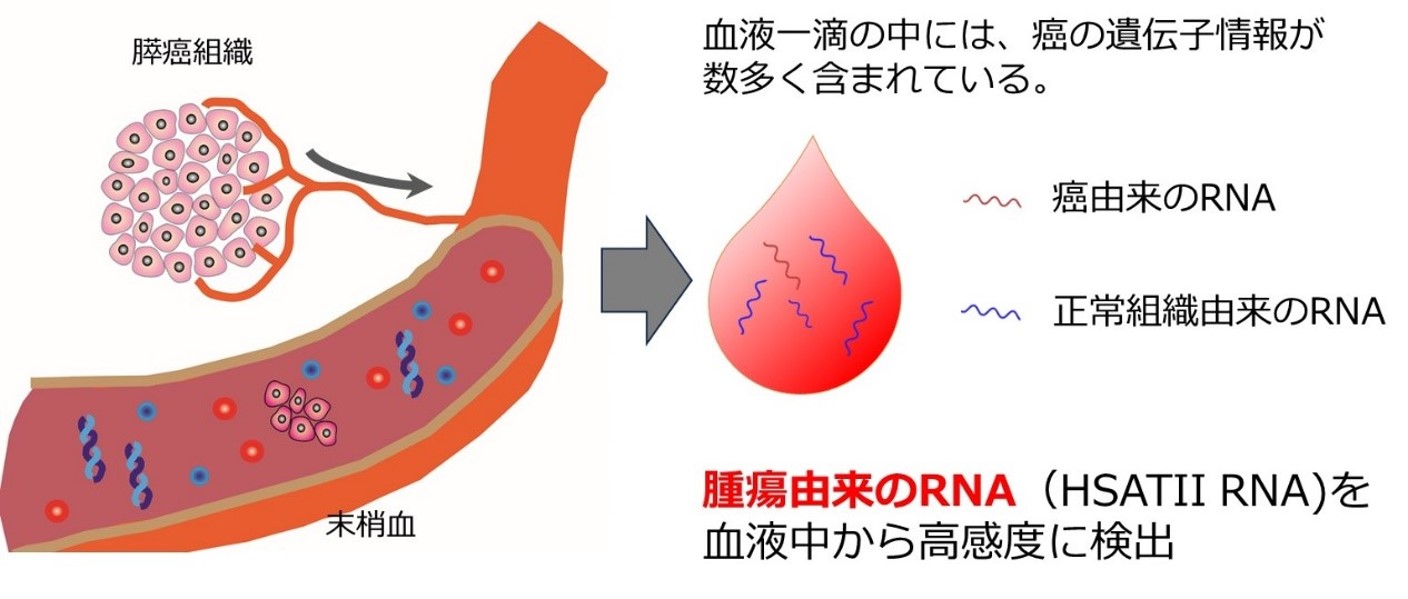
そのため、私たちは増加の一途を辿っている膵のう胞の患者さんに着目して、膵がん早期診断のための新規バイオマーカーを探索する研究を行っています。近年がん組織からはDNAやRNAなどの種々の遺伝子情報が、血液中に分泌・漏出してきていることが分かってきています。この情報を血液中から的確に入手することによって、直接腫瘍組織にアプローチすることなく、非侵襲的にがんの存在・特性を知ることができるようになってきました。私たちは膵がんで異常に作られているHSATII とよばれる特殊な反復配列RNAの定量法を独自に開発し、膵のう胞の患者さんにおける膵がん早期診断のためのサーベイランス法について研究しています。この研究により、膵のう胞の患者さんに生じる可能性がある膵がんを、より早期により低侵襲に診断できるようなると期待しています。
切除不能・再発胆道がんに対する薬物療法について
前述のように胆道がんの多くは切除不能な状態で診断され、また術後再発も多いことから、抗がん剤による薬物療法が胆道がん治療の中心的な役割を果たしています。従来は胆道がんに対する薬物療法として細胞障害性性抗がん剤 (がん細胞に作用し、細胞の増殖を抑える薬)のみが使用可能でしたが、2022年12月より免疫チェックポイント阻害剤であるデュルバルマブが、細胞障害性性抗がん剤であるゲムシタビン・シスプラチンとの併用で使用可能になりました。
免疫チェックポイント阻害剤は、 PD-1 (患者のTリンパ球に発現)と PD-L1 (がん細胞に発現)の結合を阻害する事で、患者自身が持っているTリンパ球が、がん細胞を攻撃できるようにする薬のことです。現在、デュルバルマブ以外にも様々な免疫チェックポイント阻害剤が盛んに開発されており、固形がんに対する薬物療法の中心的存在になりつつあります。
免疫チェックポイント阻害剤の作用機序
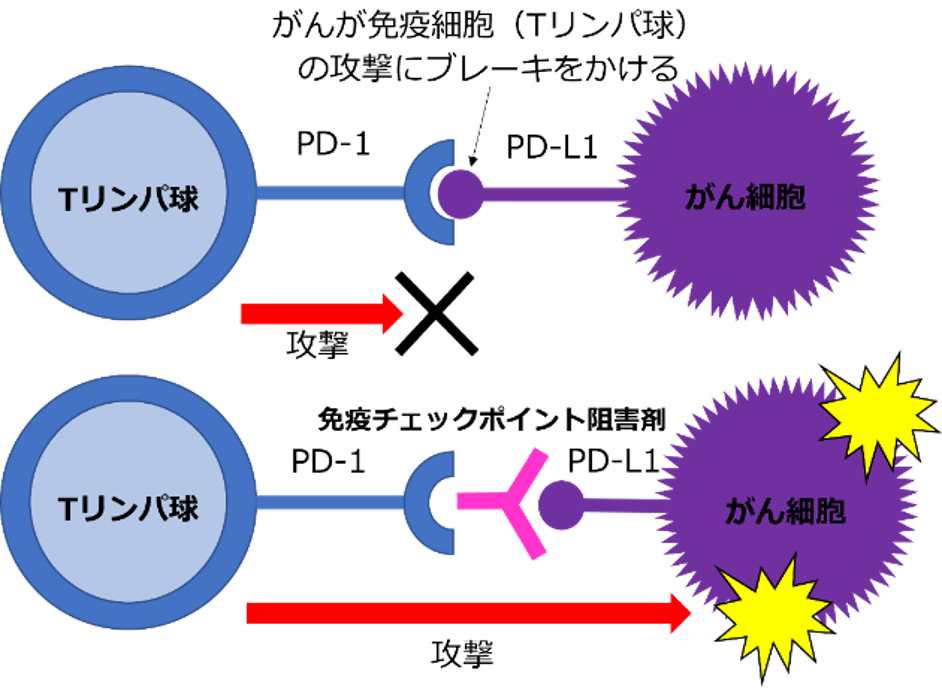
免疫チェックポイント阻害剤の奏功を予測する因子として様々なものが知られていますが、近年腸内細菌叢が免疫チェックポイント阻害剤の奏功に大きく関わることが報告されています。整腸剤として知られている酪酸菌製剤を内服することで、腸内細菌叢が変化し、免疫チェックポイント阻害剤が奏功するということが、さまざまながんで報告されています。そのため、胆道がんにおいても免疫チェックポイント阻害剤に酪酸菌製剤を併用することにより、治療効果の向上が期待されています。
私たちは、ゲムシタビン・シスプラチン・デュルバルマブ併用療法に酪酸菌製剤を併用する臨床試験を進めています。
新しい抗がん剤治療である腹腔内化学療法や酪酸菌製剤併用の免疫チェックポイント阻害剤の有効性を示すことができれば、より多くの患者さんの助けになる可能性があります。更にこれらの治療効果や耐性獲得についての解析により、さらなる新規治療の開発につながる知見が得られるものと期待しています。
これらの研究は公的な競争的資金や東京大学医学部附属病院の研究費を用いて実施していますが、より質の高い研究を迅速に実施するためには、更に研究費が必要です。最難治がんである胆膵がんに対する早期診断・新規治療の開発に向けた研究に対する、皆様のご支援を賜りますようお願い申し上げます。
基金設立3年間の経過報告
2026年01月22日(木)

平素より、「胆膵がんに対する早期診断および新規治療法の研究開発」に対し、長年にわたり温かいご支援を賜り、心より御礼申し上げます。
本基金は設立から3年が経過し、皆様からのご寄付を基盤として、胆膵がん領域における基礎的検討から臨床応用を見据えた研究を段階的に推進してまいりました。本報告では、基金設立以降の主な取り組みと研究の進展についてご報告申し上げます。
【腹膜播種を伴う膵癌に対する新規治療法の開発】
基金設立当初より、予後不良で治療選択肢が極めて限られてきた腹膜播種を伴う膵癌に対し、新たな治療戦略を確立することを重要な目標の一つとして掲げてまいりました。この3年間で、腹腔内化学療法という治療コンセプトの臨床的妥当性を検証するための臨床研究を進めてきました。その結果、全身化学療法に腹腔内治療を組み合わせた治療戦略について、一定の有効性および安全性が示唆され、今後のさらなる臨床研究へと発展させるための基盤が確立されました。本治療法は、腹膜播種を有する膵癌の患者さんに対し、新たな治療の選択肢となる可能性を有しており、今後の発展が期待されます。
【膵がん早期診断を目指したバイオマーカー研究】
膵がんの予後改善には、治療成績の向上と同時に、より早期の段階で疾患を捉える診断体系の確立が不可欠です。本基金では設立当初より、膵がん高危険群に着目した早期診断研究を重点課題として取り組んでまいりました。
この3年間で、2,000名を超える膵のう胞患者さんの臨床情報・画像データを体系的に集積した大規模データベースを構築し、膵発がんリスク因子の解析基盤を整備しました。その過程で、脂肪膵と膵がん発症との関連に着目した研究を進め、膵のう胞患者さんにおける発がんリスク評価に新たな視点を提供する知見が得られました。詳細は東大病院からプレスリリースされた以下の記事をご参照ください (https://www.h.u-tokyo.ac.jp/press/20250604-2.html)。
これらの成果は、膵がんのリスク層別化や、将来的な個別化サーベイランス戦略の確立につながる重要な一歩であり、膵がん早期診断研究の基盤形成として大きな意義を有しています。
【寄付金の活用と研究基盤の整備】
皆様からお寄せいただいた寄付金は、研究用試薬・機器の整備、臨床研究に必要な倫理審査・研究支援体制の構築、データベース管理、ならびに研究成果の学術発信など、研究推進の基盤整備に有効に活用させていただきました。
これらのご支援により、継続的かつ質の高い研究を行うための環境を整えることができましたこと、改めて深く感謝申し上げます。
【今後に向けて】
胆膵がんは現在もなお最難治がんの一つであり、克服すべき課題は多く残されています。本基金設立からの3年間で築き上げた研究基盤と知見を礎に、今後はより実臨床に還元可能な研究へと発展させていくことが求められます。私たちは引き続き、胆膵がんに苦しむ患者さんの未来を切り拓くことを目標に、研究・臨床の両面から全力で取り組んでまいります。今後とも、本基金の趣旨にご賛同いただき、変わらぬご理解とご支援を賜りますよう、何卒よろしくお願い申し上げます。
2025年活動報告
2025年12月17日(水)
平素より、胆膵がんに対する早期診断および新規治療法の研究開発に格別のご支援を賜り、心より御礼申し上げます。
皆様からのご寄付を活用して進めている研究プロジェクトの進捗と成果についてご報告申し上げます。
1. 腹膜播種を伴う膵癌に対する新規治療法の開発
本プロジェクトの一環として、腹膜播種を伴う膵癌患者さんを対象とした腹腔内化学療法の臨床研究を実施してまいりました。ゲムシタビン/ナブ-パクリタキセル併用療法にパクリタキセル腹腔内投与の臨床研究が終了し、総括報告書を第181回先進医療技術審査部会に提出しました。一定の有効性および安全性が確認され、今後より多数例を対象とした比較試験を実施する価値のある治療法であることが評価されました。
腹膜播種を伴う膵癌は、これまで有効な治療選択肢が極めて限られてきました。本治療法を腹膜播種に対する新たな治療選択肢の一つとして確立できれば、治療に苦慮されている多くの患者さんに新たな希望を届けることができると考えています。
2. 膵がん早期診断を目指したバイオマーカー研究
膵がんの予後改善には、早期診断の確立が不可欠です。当科ではその実現を目指し、膵がん早期診断のためのバイオマーカー確立に関する研究を進めています。私たちは現在2,000名以上の膵のう胞患者さんを対象とした大規模データベースを構築し、膵のう胞に伴う膵発がんの危険因子に関する研究を進めています。
その成果の一つとして、膵のう胞の長期経過観察開始当初から脂肪膵を認める患者さんでは、IPMN併存癌を発症しやすいことに加え、脂肪膵の程度が高度であるほど、IPMN併存癌のリスクが高くなることを明らかにしました。本研究はIPMN由来癌とIPMN併存癌の発生機序の違いに迫った点、脂肪膵と通常型膵癌の発生との因果関係を明確に示した点において高い新規性を有しており、今後の膵癌リスク層別化や早期発見に大きく貢献する成果であると考えています。
将来的には、膵のう胞患者さんに対するより効率的かつ適切なサーベイランス体制の確立のみならず、膵がんそのものの早期診断につながることが期待されます。
3. 今後に向けて
これらの研究は、主に公的な競争的研究資金および東京大学医学部附属病院の研究費を用いて実施してまいりました。しかしながら、より質の高い研究を、より迅速に推進するためには、さらなる研究資金が不可欠です。胆膵がんは依然として最難治がんの一つであり、早期診断法や新規治療法の開発は喫緊の課題です。今後も私たちは、胆膵がんに苦しむ患者さんの未来を切り拓くべく、研究・臨床の両面から全力で取り組んでまいります。引き続き、本研究への温かいご理解とご支援を賜りますよう、何卒よろしくお願い申し上げます。
2024年活動報告
2025年01月14日(火)

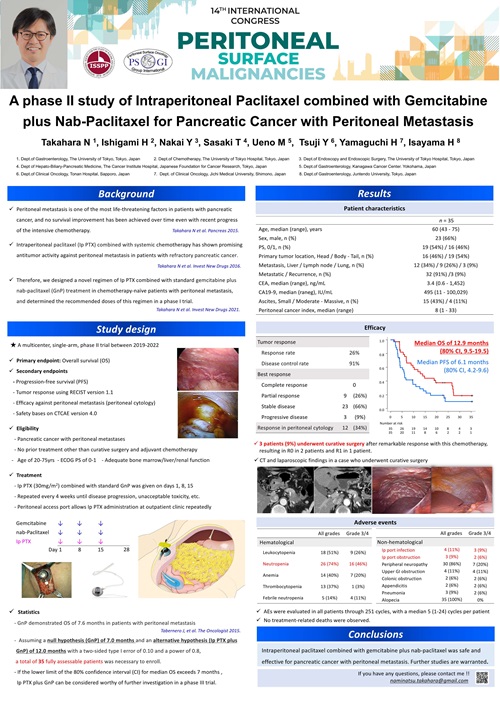
本プロジェクトのひとつとして、腹膜播種を伴う膵癌の患者さんを対象とした腹腔内化学療法の臨床研究 (ゲムシタビン/ナブ-パクリタキセル療法+パクリタキセル腹腔内投与併用療法の第2相試験) を行ってきました。ご参加いただいた患者さんの研究治療期間が終了し、治療成績を2024年7月に宇都宮で開催された第55回 日本膵臓学会および9月にフランスのリヨンで開催された第14回ISSPPという国際学会で報告しました。腹腔内化学療法の高い有効性および安全性が評価され、ISSPPではBest poster awardをいただきました(TOP写真を参照ください)。今後、腹腔内化学療法を腹膜播種に対する新たな治療選択肢のひとつに加えることができれば、腹膜播種で苦しんでいる患者さんのお役に立てるものと考えています。
また、膵がん早期診断のためのバイオマーカーの確立を目指した研究も順調に進んでいます。膵がん検診の広がりに伴い、特に膵のう胞を新規に指摘される患者さんが増えています。当科ではこれまでに2,000名以上の膵のう胞患者さんの診療にあたり、臨床情報を蓄積してきました。この多数の患者さんを長期間フォローしている大規模なデータベースは、世界でも他に類を見ないものとなっています。私たちはこのデータベースを用いて、膵のう胞に伴う膵発がんの危険因子に関する重要な臨床疫学的知見を見出し、国内外の学会および英文医学雑誌に報告してきました。今後、膵の胞患者さんの効率的なサーベイランスの確立だけでなく、膵がん早期診断にも役立つことが期待されています。
これらの研究は公的な競争的資金や東京大学医学部附属病院の研究費を用いて実施していますが、より質の高い研究を迅速に実施するためには、更なる研究費が必要不可欠です。今後も最難治がんである胆膵がんに対する早期診断・新規治療の開発に向けた研究に対する皆様のご支援を宜しくお願い申し上げます。
2023年活動報告
-早期診断・新規治療の開発に向けた研究を進めています-
2024年01月23日(火)
本プロジェクトのひとつとして、腹膜播種を伴う膵癌の患者さんを対象とした腹腔内化学療法の臨床研究を行ってきました。2020年からゲムシタビン/ナブ-パクリタキセル療法+パクリタキセル腹腔内投与併用療法の有効性および安全性を評価するために、東京大学医学部附属病院をはじめとする全国6施設による多施設共同研究を実施し、目標症例数の登録を完了することができました。現在ご参加いただいた患者さんの治療を継続し、2024年6月に試験結果を解析する予定です。私たちは腹腔内化学療法の高い有効性を実感しており、腹腔内化学療法を保険適応の治療のひとつに加えることができれば、腹膜播種で苦しんでいる患者さんのお役に立てるものと考えています。
また膵がん早期診断のためのバイオマーカーの確立を目指した研究も進めています。これまでに私たちは膵がんで異常に作られているHSATII とよばれる特殊な反復配列RNAの定量法を独自に開発しました。現在、膵のう胞患者さんの血液サンプルを用いて、診断精度のさらなる向上を目指した改良が進行中です。
これらの研究は公的な競争的資金や東京大学医学部附属病院の研究費を用いて実施していますが、より質の高い研究を迅速に実施するためには、更なる研究費が必要不可欠です。最難治がんである胆膵がんに対する早期診断・新規治療の開発に向けた研究に対する皆様のご支援を宜しくお願い申し上げます。



















<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
些少ですが研究に役立ててください。
<胆膵癌に対する早期診断・新規治療の研究開発>
ほんの少しの額ですが、助かるがんになるための研究に協力させてください。
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>
<胆膵癌に対する早期診断・新規治療の研究開発>